

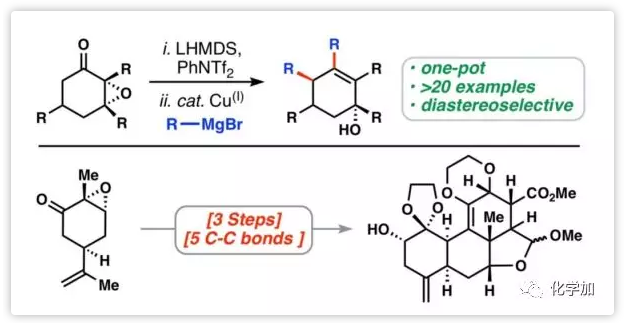
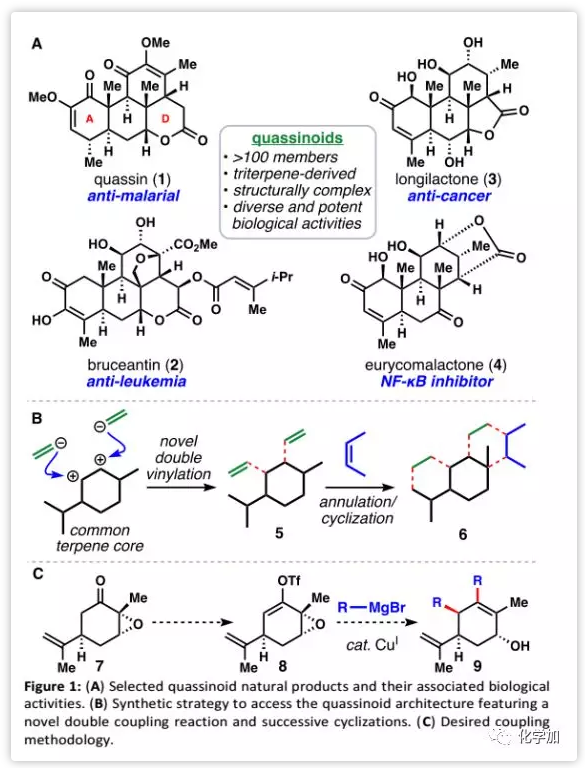
快速構建復雜天然產物分子一直是有機合成的主要推動力,特別是對于高度復雜天然產物的合成簡化。苦味堿類天然產物,由三萜衍生而來,其結構特征在于通常含有一個D-環內酯的四環體系(1-4, Figure 1A)。此外,許多苦味堿類天然產物具有顯著的生物學特征-特別是有效的抗癌活性。因此,該類天然產物分子一直是有機合成化學家的合成目標。
由于先前已經確定了一種手性源單萜的雙重乙烯基化轉化途徑,加州大學伯克利分校Thomas J. Maimone教授課題組設想通過兩個連續的成環反應將中間體推進到苦味堿環體系(6)(Figure 1B)。受Wender課題組關于環氧烯醇醚、烯醇磷酸酯和SN2'反應中烯醇化物的各種有機金屬試劑的報道以及McMurry課題組關于乙烯基三氟甲磺酸酯與銅酸鹽交叉偶聯工作的啟發,作者設想開發一種Cu(I)催化的轉化過程,可以將香芹酮環氧化物7通過乙烯基三氟甲磺酸酯8和簡單的格氏試劑直接得到官能化的環己烯醇9(Figure 1C)。近日,Maimone課題組在Chemical Science報道了由Cu(I)絡合物催化的環氧酮與格氏試劑的雙重偶聯,利用該反應只需三步即可形成五個C-C鍵實現苦味堿母核骨架的構建。
(圖片來源:Chemical Science)
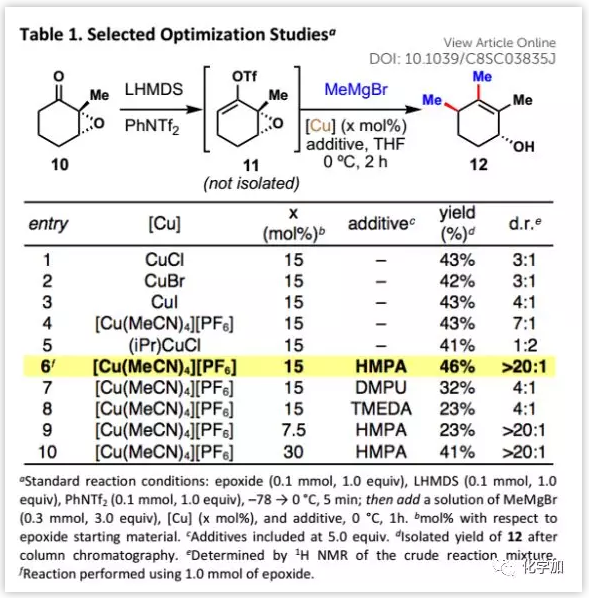
首先,作者用環氧酮10與甲基格氏試劑偶聯制備雙重偶聯產物12作為模型反應進行了研究(Table 1)。其中,乙烯基三氟甲磺酸酯中間體11無需分離;隨后,作者發現雖然非對映選擇性水平不同,但多種Cu(I)鹽均能夠催化這種轉化。大多數Cu催化劑能夠實現烯丙基取代的預期反式立體化學;然而,當Cu中心與龐大的NHC配體連接時,卻得到順式立體化學。在所有銅源中,[Cu(MeCN)4][PF6]效果最好,被用于進一步研究。
極性添加劑可能會影響非對映選擇性,特別是發現HMPA幾乎將烯丙基全部變為反式異構體。改變催化劑負載量對非對映選擇性沒有明顯影響,但當負載量低于15 mol%時,則對產率產生不良影響。
(圖片來源:Chemical Science)
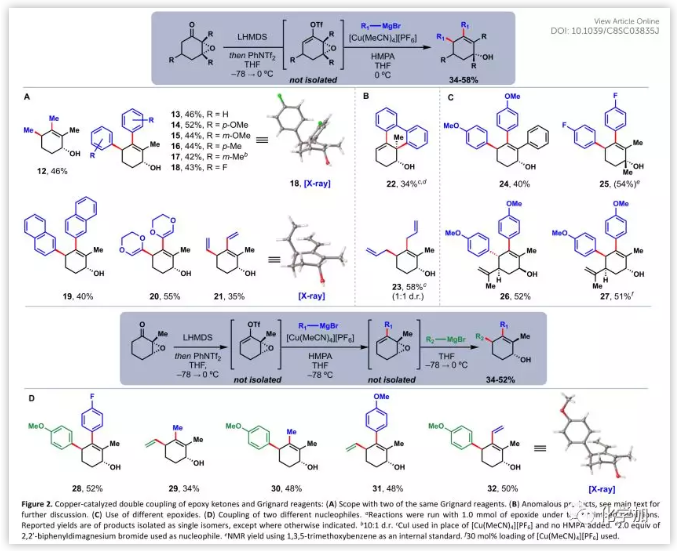
接下來,作者開始探索這種串聯偶聯過程的適用范圍(Figure 2A)。通過實驗發現,具有不同取代基的芳香格氏試劑利用該轉化可以高純度和收率得到相應的產物,其他與苦味堿合成有關的sp2親核試劑如二烯醇基和乙烯基也可以偶聯產生單一非對映異構體,18和21的單晶X射線衍射分析證實了反式立體化學。以下兩種底物需要指出(Figure 2B):首先,由于可能是分子內的或非催化的過程,衍生自2,2'-二溴聯苯的二格氏試劑時形成的產物22僅經歷了環氧化物的交叉偶聯和SN2開環;其次,由于試劑的高親核性,烯丙基格氏試劑的偶聯產物23為順式和反式非對映異構體的1:1混合物。
該方法還可以耐受不同的環氧化物底物(Figure 2C)。用較大的苯基取代2-甲基或在3-位引入甲基不會影響相應的產物生成(24,25)。然而,該化合物的叔烯丙醇片段對酸高度敏感,易發生脫水反應。香芹酮環氧化物的兩種非對映異構體也可以干凈得到相應的產物(26,27)。另外,該反應可以克服cis-香芹酮環氧化物的固有空間取向得到anti-27。
最后,作者將該方法進行了擴展,通過“一鍋法”與兩個不同的親核試劑進行偶聯(Figure 2D)。首先,作者發現在低溫(-78 ℃)下,可以進行選擇性交叉偶聯得到產物。當用不同的親核試劑處理該中間體,僅在加熱至0 ℃時才進行烯丙基取代。此外,親核試劑本身(芳基、乙烯基、烷基等)不會改變這種轉化的選擇性; 而控制因素是親核試劑的加入順序和反應溫度。因此,通過改變親核試劑的加料順序,可以直接得到區域異構產物31和32,通過單晶X射線衍射分析證實了32的連接和選擇性。
(圖片來源:Chemical Science)
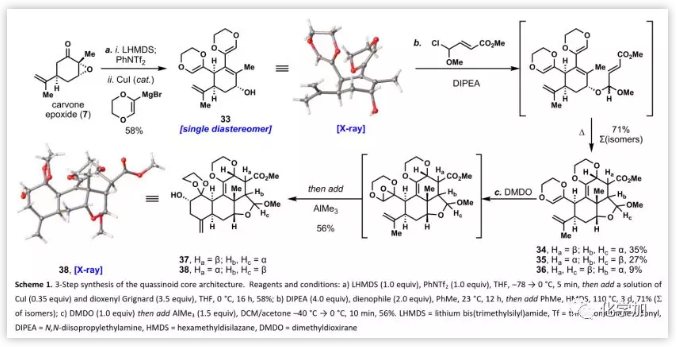
接下來,作者將注意力轉向于苦味堿環體系的構建(Scheme 1)。首先,作者將香芹酮環氧化物與基于二烯烴的Grignard試劑偶聯得到單一異構體33,通過X射線晶體學分析確定其立體化學為反式。作者認為苦味堿的C-環和D-環可以由乙烯基二氧六環片段與連接在烯丙醇33上的親二烯醇片段通過分子內Diels-Alder反應構建。由于烯丙醇在熱和酸性條件下不穩定,起初的嘗試均失敗。最后,在堿性(DIPEA)條件下,用甲基氯代烷基醚將游離醇烷基化產生一對非對映異構縮醛(d.r. 1:1),然后加熱進行Diels-Alder反應。實驗發現,縮醛立體化學對環加成反應的內/外式選擇性具有很強的控制作用,即一種縮醛異構體只產生內式產物(34),而另一種產生exo-35優于endo-36(3:1 exo:endo),分離得到兩種主要的非對映異構體endo-34和exo-35,其中通過單晶X射線衍射分析證實35為外式產物。
對于苦味堿母核的合成,作者設想通過級聯二烯烴氧化/重排/環化構建A環。Hanna及其同事之前報道,取代的二烯烴的環氧化和重排成醛很容易進行。作者在實驗中發現,通過用DMDO處理,然后加入Lewis酸可以得到干凈的環氧化物中間體(Scheme 1);并且,三甲基鋁是兩種轉化的最佳Lewis酸,可以56%的總產率得到仲醇37和38。隨后,以相當的效率得到兩種烯產物,并且在新形成的醇立體中心為單一異構體。38的立體化學通過單晶X射線晶體學分析進一步證實。至此,僅通過三步就完成了苦味堿母核結構的構建,其中構建了五個C-C鍵和七個手性中心。
(圖片來源:Chemical Science)
小結:Thomas J. Maimone教授課題組開發了一種新型的銅催化雙重官能化反應,將易得的環氧酮轉化為高度取代的非對映異構純的烯丙基醇,并將其用于快速構建(僅三步)苦味堿母核結構中。該轉化具有廣泛的底物范圍,包括各類親核試劑和環氧化物。作者開發的方法有助于快速獲取高價值的中間體和其他復雜的天然產物結構以及合成多種苦味堿類天然產物。
撰稿人:爽爽的朝陽
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn