

近日,浙江大學孫斐/于興華團隊,聯合深圳大學王東/燕鼎元團隊在Biomaterials雜志上在線發表了題為Blood-testis barrier-crossing extracellular vesicles for asthenospermia therapy via synergistic ATP replenishment and ferroptosis suppression的研究新成果。該研究成功構建了一種多功能細胞外囊泡,實現了在可視化追蹤下高效穿越血睪屏障,并通過能量補充與鐵死亡抑制的協同機制,顯著改善弱精癥模型的精子數量與活力。

男性不育中,弱精癥(精子活力不足)是主要原因之一。其治療一直面臨著一個核心難題:人體為了保護生精環境而設立的血睪屏障,在阻擋有害物質的同時,也嚴重阻礙了絕大多數治療藥物的進入,導致傳統療法效果甚微。
為解決這一難題,研究團隊獨辟蹊徑,從人臍帶間充質干細胞中提取了天然的“快遞小車”——細胞外囊泡,并對其進行精密“改造”:
裝載“能量電池”——ATP:將三磷酸腺苷(ATP)封裝進囊泡,直接為精子產生過程中的細胞“充電”,解決其能量枯竭的核心問題。
安裝“追蹤器”——NIR-II AIEgens: 利用具有聚集誘導發光特性的材料,為囊泡裝上NIR-II熒光“導航燈”。這使得研究人員能夠清晰地觀看這些囊泡如何穿越復雜的血睪屏障,并精準抵達生精小管靶區。
啟動“保護程序”——抑制鐵死亡: 研究揭示,這些工程化的囊泡本身還能上調睪丸組織內的關鍵抗氧化蛋白GPX4,從而有效抑制“鐵死亡”這一細胞死亡方式,保護生精細胞免受氧化應激損傷。
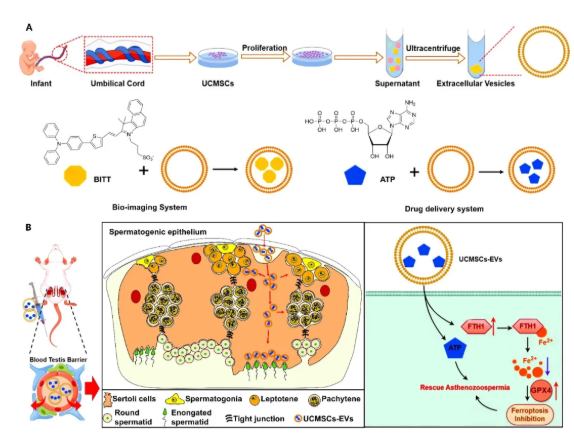
“可視化”與“雙管齊下”的治療策略
本研究引人注目的亮點在于,它并非一次盲目的“藥物遞送”,而是一次全程可控、路徑清晰的“精準醫療”。通過先進的NIR-II成像技術,團隊證實了工程化囊泡能夠高效富集于睪丸組織。
更為重要的是,該平臺展現了一種“雙管齊下”的協同治療機制:一方面, 釋放的ATP直接補充了生精細胞的能量庫,快速提升了精子活力;另一方面, 囊泡介導的GPX4上調,構筑了強大的細胞保護屏障,通過抑制鐵死亡有效增加了精子數量。兩者協同,從根本上針對弱精癥的病因(能量不足與氧化損傷)進行了聯合打擊。
動物實驗結果表明,該療法能顯著改善弱精癥模型的各項關鍵指標,包括精子數量、前向運動能力和運動速度,且未觀察到全身毒性,展現出優異的生物安全性。
原文鏈接:https://www.sciencedirect.com/science/article/pii/S0142961225006969
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn