

上海交通大學陳志敏課題組長期致力于手性有機硫/硒化學研究,近年來開發了Lewis堿/Br?nsted酸協同催化烯烴的親電硫化/硒化反應,高效合成了一系列中心手性有機硫/硒化合物(Angew. Chem. Int. Ed., 2025, 64, e202503815; Nat. Commun., 2025, 16, 2147; Angew. Chem. Int. Ed., 2019, 58, 12491-12496; CCS Chem., 2022, 4, 3342-3354; ACS Catal. 2023, 13, 2715-2722.)。同時,他們于2022年首次實現了Lewis堿催化的芳香親電硫代反應,為合成軸手性含硫化合物提供了新方法(J. Am. Chem. Soc., 2022, 144, 2943-2952; Angew. Chem. Int. Ed., 2022, 61, e202211782.)。并進一步將該策略拓展至平面手性含硫大環化合物與固有手性含硫杯芳烴的高效構筑(Angew. Chem. Int. Ed., 2024, 63, e202318625; Nat. Commun., 2024, 15, 9929.)。近期,該課題組取得新進展,報道了基于動態動力學拆分策略的不對稱親電硫代反應,成功實現了螺旋手性含硫氮雜-[5]螺烯的高效、高對映選擇性合成 。
螺旋手性化合物因其獨特的結構與電子性質,在功能材料與不對稱催化等領域應用潛力廣闊(Scheme 1a)。盡管合成化學家已發展了多種方法以構建結構多樣的手性螺烯,但與發展相對成熟的中心手性及軸手性不對稱合成相比,其催化不對稱合成研究仍面臨挑戰,關注相對較少(Scheme 1b)。這一挑戰可能主要源于其螺旋骨架固有的結構剛性與較大空間位阻,使得高對映選擇性構建較為困難。現有策略主要包括從頭合成、動力學拆分及動態動力學拆分;其中,DKR策略雖簡捷高效,但目前僅有一例相關研究報道(Scheme 1c)。此外,有機催化在該領域的應用也相對滯后。因此,發展新策略以高效合成具有獨特結構的螺旋手性分子,仍是當前亟需解決的重要課題。
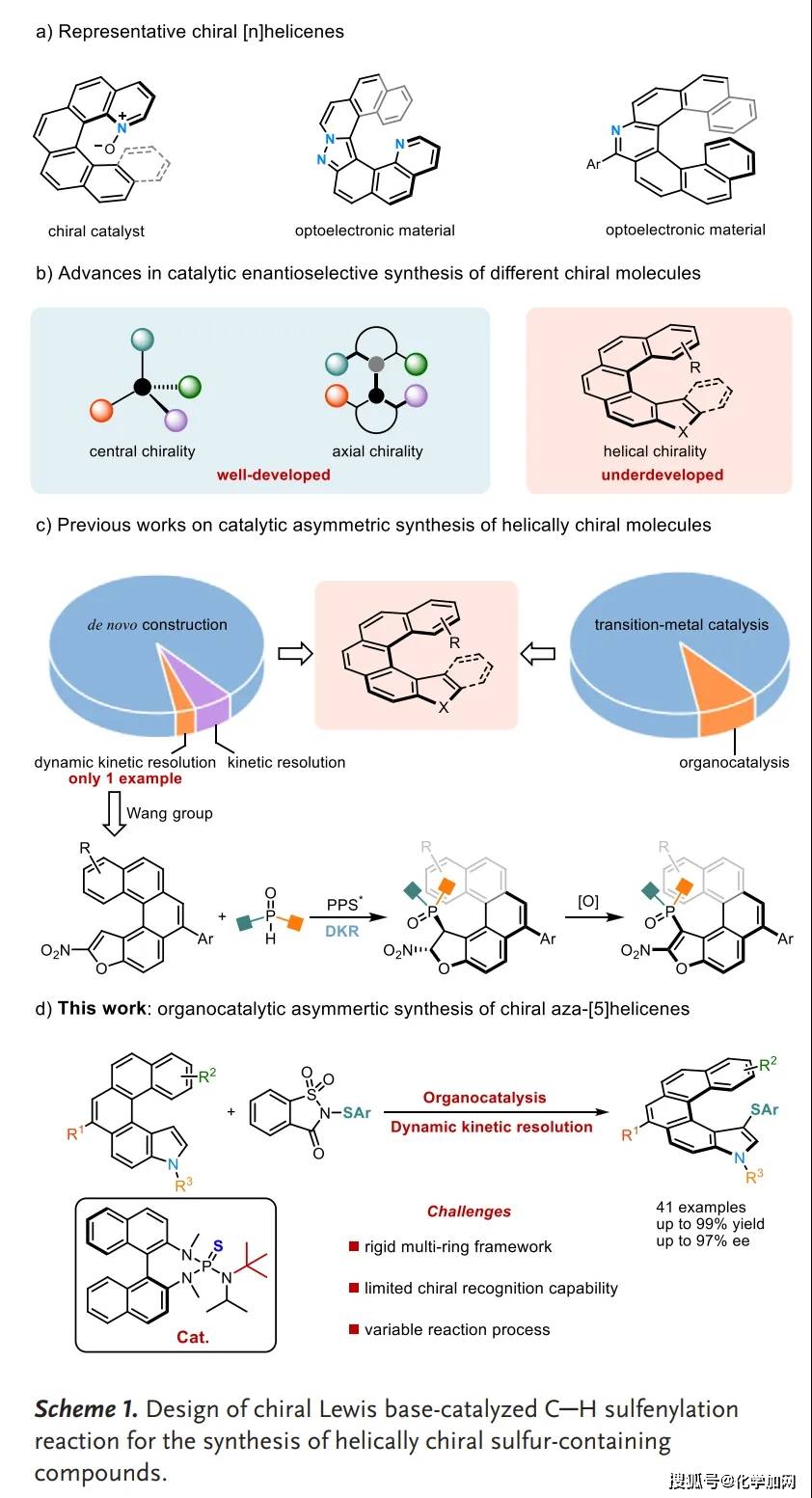
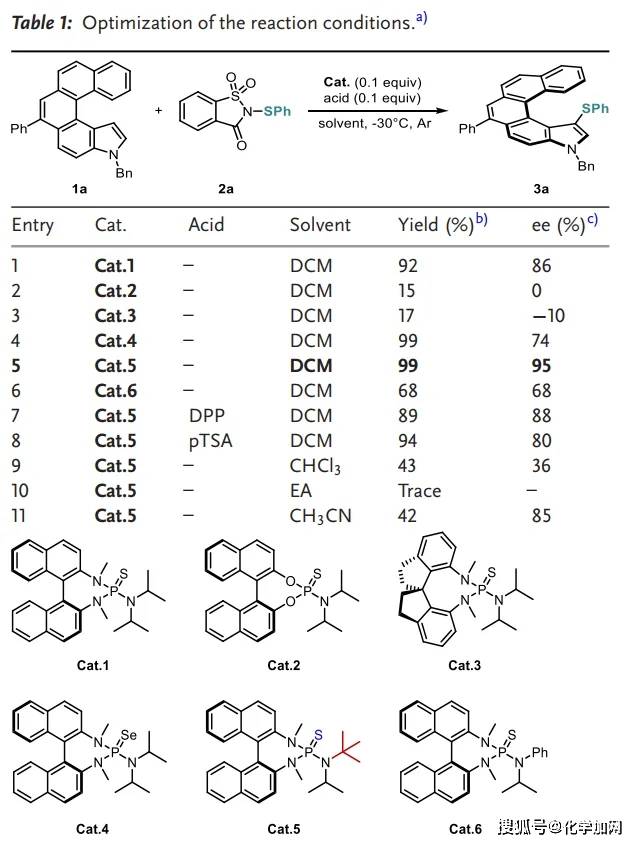
本研究設計通過吲哚衍生物的C–H硫化反應來高效構建結構多樣的螺旋手性含硫氮雜-[5]螺烯(Scheme 1d)。首先使用一種新型吲哚衍生物1a作為模型底物,并選用糖精衍生的硫化試劑2a作為親電試劑。初始反應在手性BINAM衍生Lewis堿催化劑Cat.1的催化下,在–30 °C、二氯甲烷(DCM)中進行(Table 1)。令人欣喜的是,目標產物3a收率達92%,86% ee。為進一步提升對映選擇性,作者對一系列催化劑、溶劑和酸進行了系統篩選,確定了最優反應條件(entry 5)。
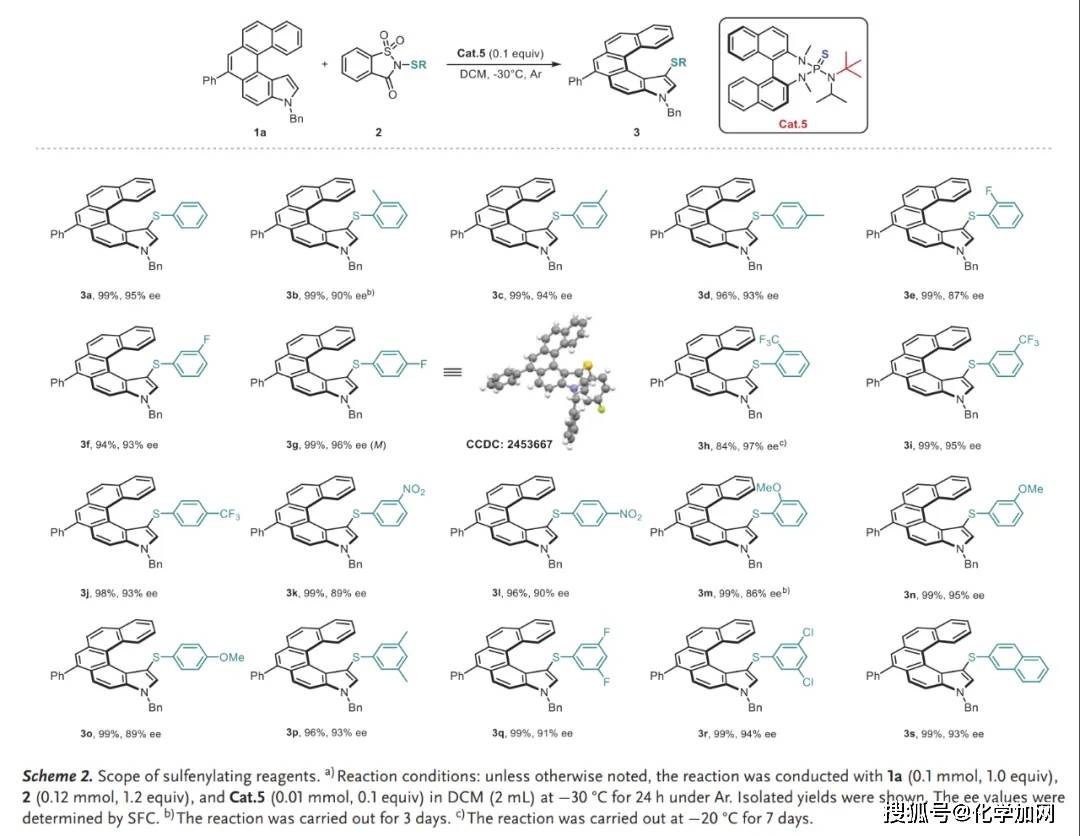
在獲得最優反應條件后,作者對該方法的底物適用性進行了考察。該方法對硫化試劑和吲哚底物均表現出廣泛的適用性。各種取代的糖精衍生硫化試劑(含甲基、氟、三氟甲基、硝基、甲氧基等取代基)以及多取代和2-萘取代的硫化試劑都能很好地適應此催化體系(Scheme 2)。同時,多種吲哚衍生物,包括帶有吸電子基團(氟、氯、氰基、酯基、三氟甲基)和給電子基團(甲氧基、羥基)的底物,以及含有2-萘環、噻吩環和烷基的底物,都能以高收率和高對映選擇性得到相應產物(Scheme 3)。
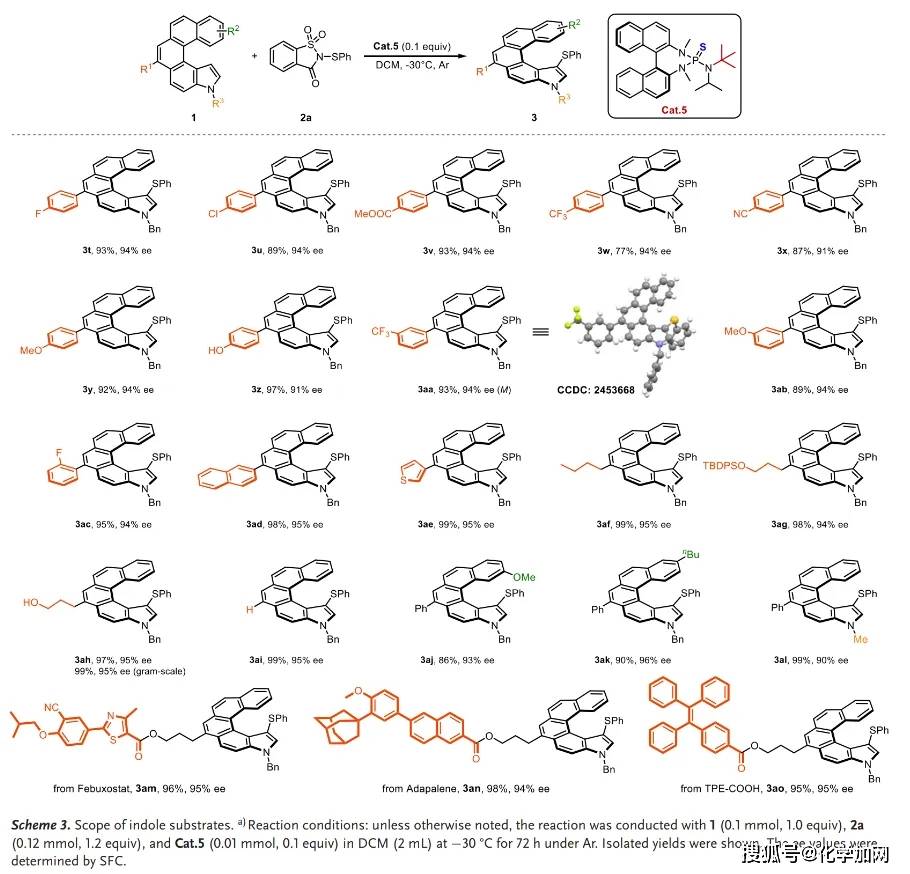
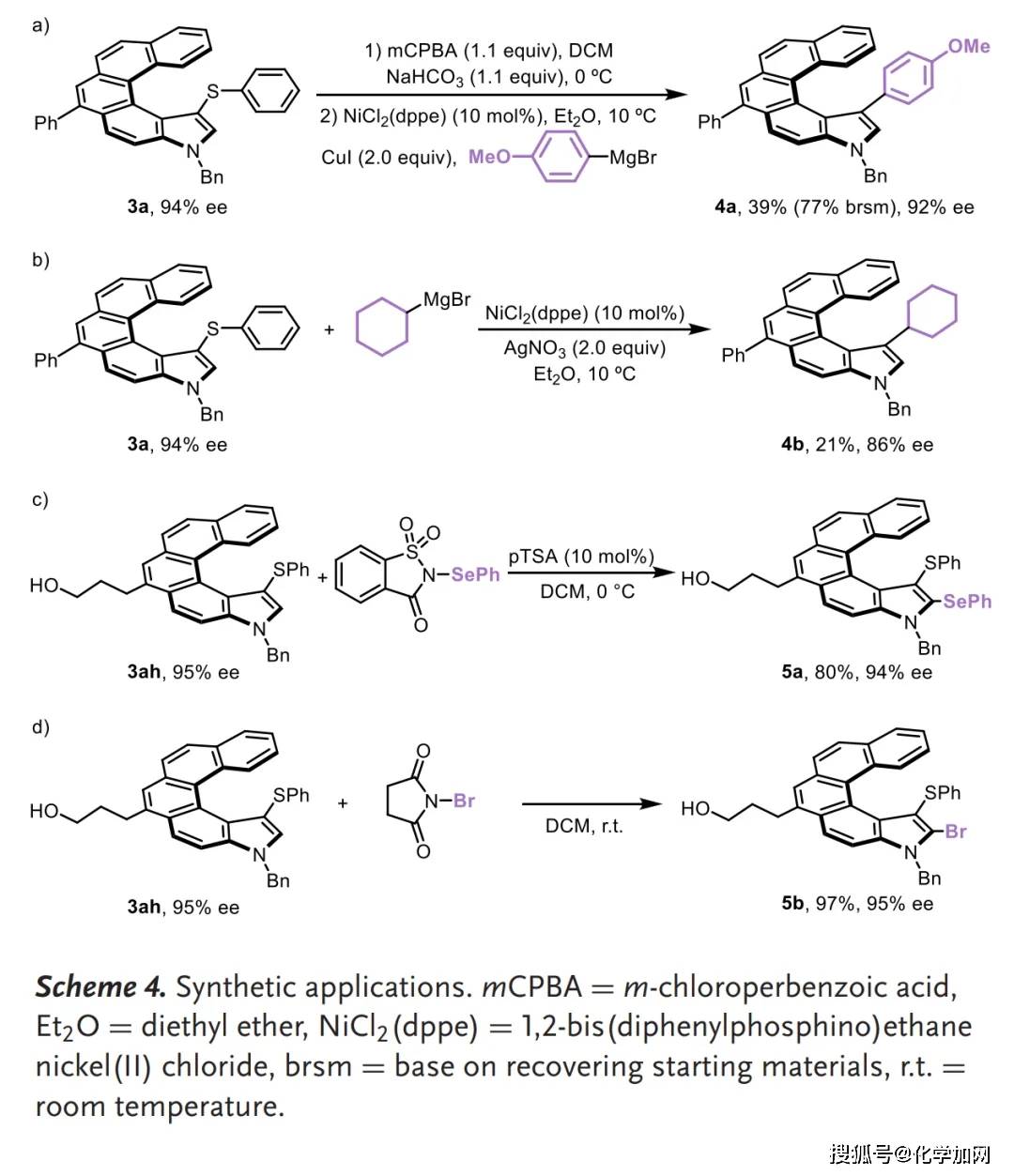
該方法也可以應用于藥物分子(如非布索坦和阿達帕林衍生物)和聚集誘導發光(AIE)分子(四苯基乙烯衍生物)的后期修飾。克級規模反應也能以99%的收率和95%的對映選擇性獲得產物3ah(Scheme 3)。此外,產物3a經過氧化和鎳催化的交叉偶聯反應,成功實現了C-S鍵斷裂和C-C鍵形成,得到了對應的芳基化和烷基化產物。化合物3ah 分別與N-苯硒代糖精 和N-溴代丁二酰亞胺(NBS) 反應也能以較高收率獲得對應取代產物且對映選擇性得以保持(Scheme 4)。
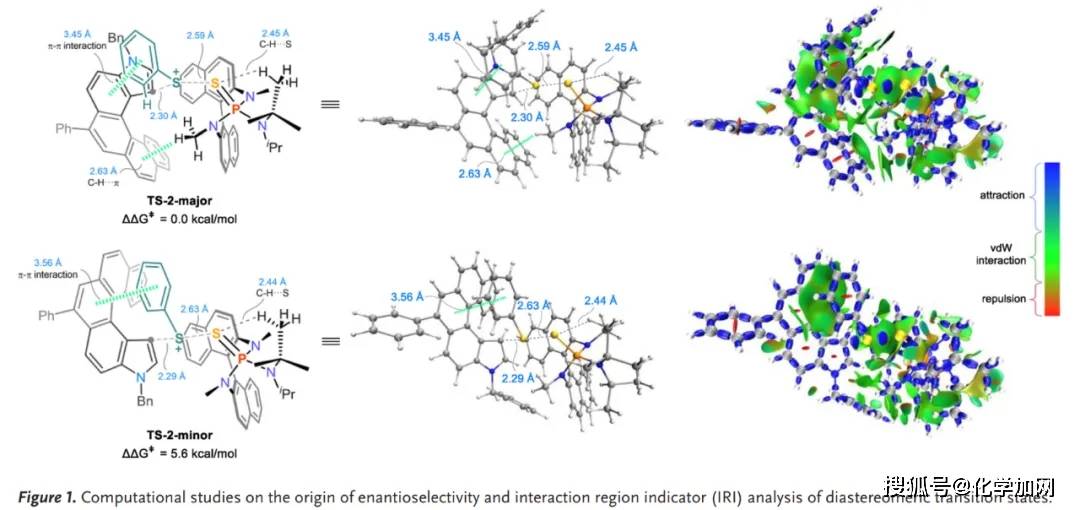
作者通過實驗證明了底物1a具有較低的旋轉能壘,容易發生外消旋化,表明芳香硫化反應通過動態動力學拆分過程進行。為深入理解反應得對映選擇性控制,作者進行了 DFT 計算,比較了兩種可能過渡態(TS-2-major 與TS-2-minor)的 Gibbs 自由能,對應于 3a 主要對映體的TS-2-major 比TS-2-minor 穩定5.6 kcal mol?1。相互作用區域指示(IRI)分析顯示TS-2-major 中存在芳基硫與底物芳環的π???π 堆積作用,催化劑 N-甲基 C–H 與底物芳環的 C–H???π 作用與催化劑與底物間顯著的范德華(vdW)作用也降低了此過渡態的能量。上述多重非共價作用的協同差異,共同決定了 TS-2-major 的能量優勢,從而保證了高對映選擇性(Figure 1)。
上海交通大學陳志敏教授課題組開發了一種通過手性硫醚催化的C-H鍵硫化反應合成螺旋手性含硫氮雜-[5]螺烯的簡便高效方法。機理研究表明該反應經歷了動態動力學拆分過程,同時DFT計算闡明了對映選擇性的起源,并強調了硫化試劑與底物之間的π-π相互作用以及催化劑與底物之間的C-H···π相互作用在此反應中的關鍵作用。該方法為螺旋手性化合物的合成提供了新策略,并在藥物分子和功能材料分子的后期修飾中展現出良好的應用潛力。該研究成果近期發表在國際學術期刊Angew. Chem. Int. Ed.上。上海交通大學李澤龍同學為該工作的第一作者,陳志敏教授為通訊作者。
Dynamic Kinetic Resolution Approach to Chiral Sulfur-Containing Aza-[5]helicenes via Chiral Lewis Base Catalyzed C─H Sulfenylation.
Ze-Long Li, Yu-Xuan Huo, Qi-Sen Gao, Dr. Tong-Mei Ding, Prof. Dr. Zhi-Min Chen
Angew. Chem. Int. Ed., 2025, e202515017
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn